
Приветствуем вас на сайте Interessno.ru, наши уважаемые читатели. Хлор (Cl) – это химический элемент с атомным номером 17. Он принадлежит к 17-й группе периодической таблицы химических элементов. Это токсичный, едкий, зеленовато-желтый газ, который раздражает глаза и органы дыхания. Но что мы знаем об этом элементе еще? На самом деле, не так уж и много.
Поэтому сегодня мы это исправим. Именно для вас, наши уважаемые читатели, мы подобрали самые интересные факты о хлоре. Надеемся, информация из статьи будет полезна и детям и школьникам, которые изучают элемент на уроках химии, и их родителям.
Содержание
№1

В земных океанах содержится большое количество хлора. Если бы он выделялся в виде газа, то его вес был бы в 5 раз больше, чем вес современной атмосферы нашей планеты. В океанах содержится около 2.6х1016 метрических тонн хлора, в основном в виде хлорида натрия (NaCl).
№2

Это очень токсичный газ. Воздействие небольшого количества Cl, даже в течение короткого времени, может быть смертельным. При концентрации хлора в воздухе 3000 мг/м3 гибель человека наступает всего после нескольких вдохов.
№3

Он тяжелее воздуха. Если выпустить хлор, он ложится на грунт как одеяло и дрейфует вместе с ветром. Его использовали в качестве химического оружия в Первой мировой войне, сначала немецкая армия в 1915 года, а затем союзные войска. Однако несмотря на всю его токсичность, он оказался не таким эффективным, так как легко обнаруживался по его сильному запаху.
Он также растворяется в воде, поэтому солдаты во время химических атак могли защитить себя от отравления дыша через влажные тряпки.
№4

Он относится к группе галогенных элементов. Это второй самый легкий галоген после фтора. Как и другие галогены, он является чрезвычайно реактивным элементом, который легко образует анион. Из-за его высокой реакционной способности, он содержится в соединениях. Более того, встретить свободный газообразный хлор в природе невозможно.
№5

Он необходим человеческому организму. В организме человека он находится в виде хлорид-иона, где он регулирует осмотическое давление и pH, и способствует нормальной работе пищеварительной системы. Этот элемент попадает в человеческий организм преимущественно с солью (NaCl).
№6
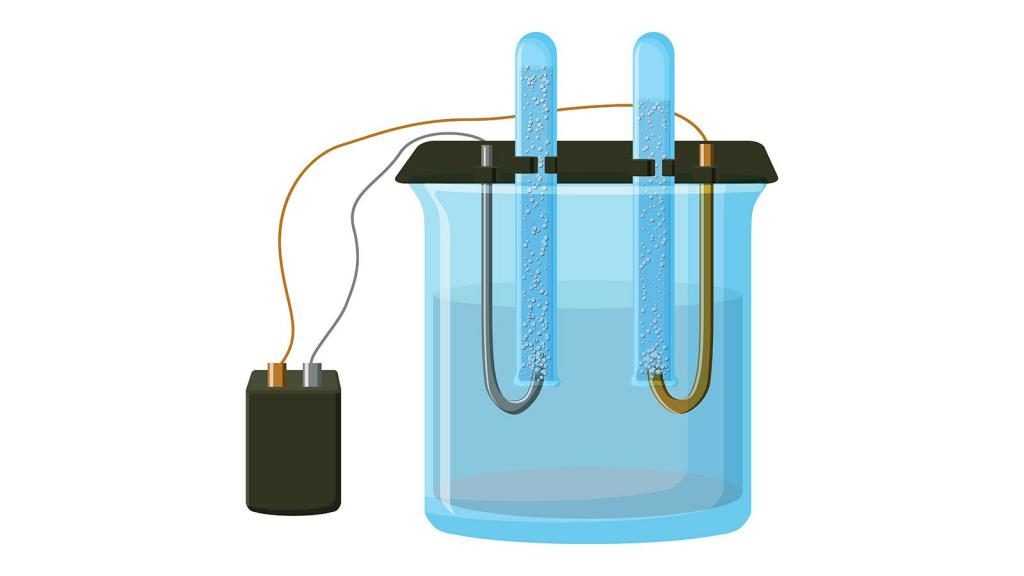
Чистый хлор получают в основном электролизом соленой воды. Он используется для очистки воды, для отбеливания, дезинфекции, обработки текстиля, а также для создания множества соединений. Что касается соединений, то к ним относятся хлораты, хлороформ, синтетический каучук и т. д.
Соединения хлора используют в медицине, пластмассах, антисептиках, инсектицидах, красках, продуктах питания и т. д.
№7

Природный хлор состоит их двух стабильных изотопов: хлора-35 и хлора-37. Что касается хлор-35, то на его долю приходится 76% от естественного содержания элемента. Хлор-37, соответственно, занимает долю в 24%.
№8

Каменная соль (она же поваренная соль) известна человечеству уже несколько тысяч лет. С древних времен соль была настоящей ценностью для людей.
В 1774 году шведский химик Карл Вильгельм Шееле смог создать зеленовато-желтоватый газ, который он не смог распознать как отдельный элемент. Он полагал, что в нем присутствует кислород. Истинная природа хлора как элемента была признана в 1810 году английским химиком Гемфри Дэви, который дал ему название хлор от греческого «chloros», которое дословно переводится как «желтовато-зеленый».
№9

Сам по себе хлор не является легковоспламеняющимся газом. Однако он может вступать во взрывоопасные реакции или образовывать взрывоопасные соединения с другими химическими веществами, такими как хлорид аммония и т.д.
№10

Это очень плотный газ с плотностью 3.21 грамма на литр. Для сравнения, плотность воздуха всего 1.29 грамма на литр. Хлор из газообразного состояния переходит в жидкое при температуре -34.05 градуса по Цельсию. Из жидкого состояния в твердое переходит при температуре -101 градус по Цельсию.
№11
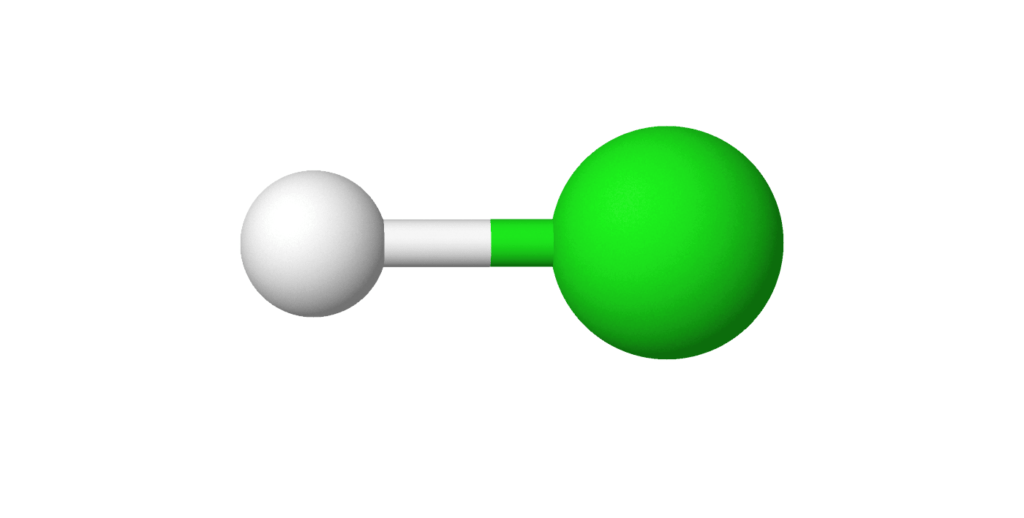
Это очень активный элемент. Он сочетается со всеми элементами, кроме благородных газов. Благородные газы входят в 18-ю группу периодической таблицы. Реакция между Cl и другими элементами может быть энергичной. Например, он вступает во взрывоопасную реакцию с водородом, с образованием хлороводорода (HCl). Сам по себе он не горит, однако как и кислород, он является хорошим окислителем.
№12
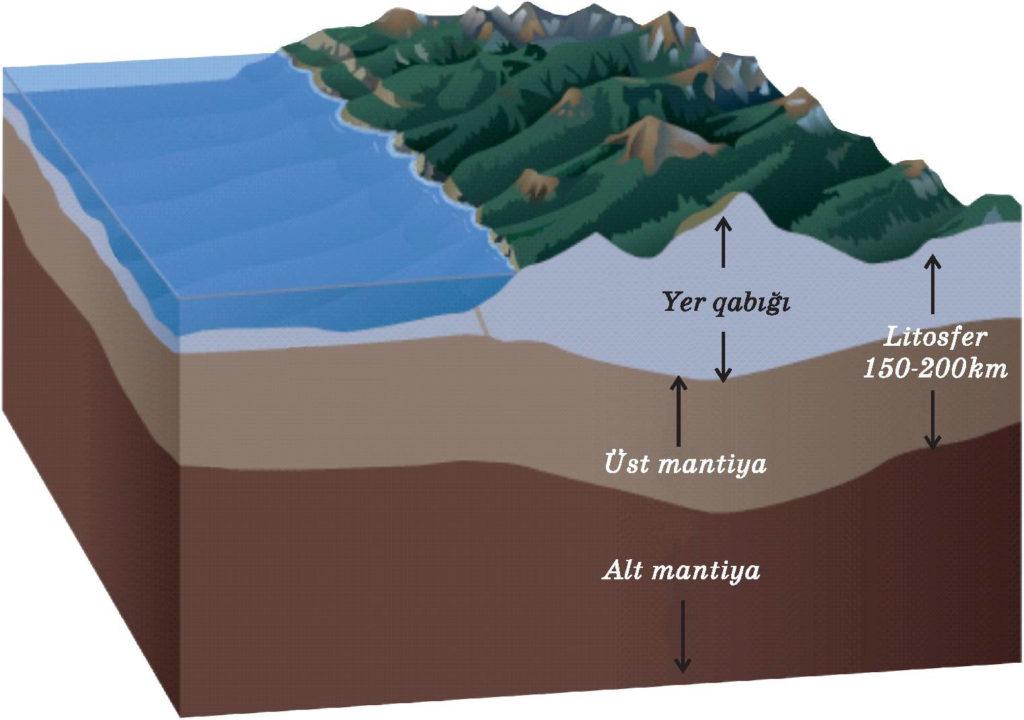
Земную кору составляет сравнительно небольшое число элементов. Приблизительно 50% приходится на кислород, а 25% на кремний. Остальные элементы занимают оставшиеся 25%. Среди эти элементов встречается и хлор. Он является 21-м самым распространенным элементом в земной коре. На его долю приходится 0.2%.
№13

Признаками нехватки хлора в организме человека являются следующие симптомы: сильное потоотделение в жару или во время физических нагрузок, рвота, расстройство пищеварительной системы, проблемы с моче-выделительной системой. Также, при нехватке этого элемента в организме, человек чувствует себя вялым, сонным, слабым и т. д. Стоит отметить, что он является девятым самым распространенным элементом в человеческом организме.
№14

Стоит отметить, что противоядия от отравления хлором нет. Если произошел контакт с жидким хлором, то нужно сразу же дезактивировать кожу и глаза обильным количеством воды.
Отравление газообразным хлором лечат с помощью увлажненного кислорода, бронходилататорами и т. д.
Рекомендуем также прочитать: Интересные факты о сере
№15

Он играет важную роль в строительной сфере. Посмотрите на ваши дома. Этот элемент был использован в производстве бетона, краски для дома, стекловолоконной изоляции и нейлонового коврового покрытия, а также пластиковых окон, водопроводных труб и напольной плитки. Практически все материалы, которые используются для строительства зданий были созданы с помощью хлора.
На этом наша статья подошла к концу, уважаемые посетители. Надеемся информация из публикации была для вас полезной и интересной. До скорых встреч.
- Интересные факты о Красной площади - 18.11.2023
- Интересные факты о Европе - 01.11.2023
- Интересные факты о клюкве - 08.10.2023
